Составление энергетических схем образования молекул и ионов
Видео:Гибридизация атомных орбиталей и геометрия молекул. 10 класс.Скачать

Энергетические схемы образования молекулы и иона водорода
Задание 76.
Нарисуйте энергетическую схему образования молекулярного нона Н2— и молекулы Н2 по методу молекулярных орбиталей. Где энергия связи больше? Почему?
Решение:
а) Энергетическая схема образования молекулярного иона Н2—:
Определим порядок связи:
Так как порядок связи равен 0,5, то ион Н2— должен быть энергетически устойчивым, по-скольку здесь из трёх электронов, которые должны разместиться на МО, два займут связывающую ( 1s), а один – разрыхляющую ( *1s) МО. Следовательно, образование иона Н2— будет сопровождаться выделением энергии. Действительно ионы Н2— экспериментально получены.
б) Энергетическая схема образования молекулы Н2:
Определим порядок связи:
Так как порядок связи равен 1, то молекула Н2 может существовать. Энергия связи в молекуле Н2 больше, чем в молекулярном ионе Н2—, так как порядок связи молекулы водорода больше Н2, чем в молекулярном ионе Н2—.
Видео:Метод молекулярных орбиталей. Часть 2. Построение энергетических схем.Скачать

Метод валентных связей
Задание 77.
Какие электроны атома бора участвуют в образовании ковалентных связей? Как метод валентных связей (ВС) объясняет симметричную треугольную форму молекулы ВЕ3?
Решение:
Атом бора на внешнем энергетическом уровне содержит два s- и один р-электрон (2s22p1). В нормальном состоянии бор проявляет ковалентность равную 1, за счёт неспаренного р-электрона может образовать ковалентную связь по обычному механизму. В возбуждённом состоянии у атома бора 2s-электрон переходит на вакантную 2р-орбиталь и при этом об-разуется три неспаренных электрона (2s12p2):
Заполнение внешнего энергетического уровня атома бора в основном состоянии:
При таком состоянии валентность (спинвалентность) атома бора равна 1.
Заполнение внешнего энергетического уровня атома бора в возбуждённом состоянии:
При таком состоянии валентность (спинвалентность) атома бора равна 3.
Атом бора образует молекулу фторида бора BF3 за счёт перекрывания электронных орбиталей, занятых неспаренными электронами, с электронными орбиталями фтора. При этом у атома бора сохраняется одна вакантная орбиталь, за счёт которой по донорно-акцепторному механизму может образовать четвёртую связь.
В атоме бора происходит гибридизация одной s-орбитали и двух р-орбиталей. В этом случае в результате линейной комбинации трёх исходных орбиталей возникают три гибридные sp2-орбитали. При перекрывании sp2-орбиталей атома бора с орбиталями трёх атомов фтора образуются три связи, равноценные по длине и энергии. Они располагаются на одной плоскости под углом 1200 друг к другу. Молекулы, в которых валентные орбитали центрального атома находятся в состоянии sp2-гибридизации, имеют форму плоского треугольника.
Энергетические схемы образования молекул кислорода, фтора и азота
Задание 78.
Нарисуйте энергетическую схему образования молекулы О2 по методу молекулярных орбиталей (МО). Как метод МО объясняет парамагнитные свойства молекулы кислорода?
Решение:
С позиций метода МО электронное строение молекулы О2 можно представить так:
Из энергетической схемы образования молекулы О2 следует, что она парамагнитна, так как на *2ру и *2рz имеются неспаренные электроны
Задание 79.
Нарисуйте энергетическую схему образования молекулы F2 по методу молекулярных орбиталей (МО). Сколько электронов находится на связывающих и разрыхляющих орбиталях? Чему равен порядок связи в этой молекуле?Решение:
С позиций метода МО электронное строение молекулы F2 можно представить так:
Из энергетической схемы образования молекулы F2 следует, что на связывающих орбиталях находится шесть электронов, а на разрыхляющих – четыре спаренных электрона. Порядок связи равен разности чисел электронов на связывающих и разрыхляющих орбиталях, делённой на два. В молекуле фтора порядок связи равен единице:
Задание 80.
Нарисуйте энергетическую схему образования молекулы N2 по методу молекулярных орбиталей (МО). Сколько электронов находится на связывающих и разрыхляющих орбиталях? Чему равен порядок связи в этой молекуле?Решение:
С позиций метода МО электронное строение молекулы N2 можно представить так:
Из энергетической схемы образования молекулыN2 следует, что на связывающих орбиталях находится шесть электронов, а на разрыхляющих – ни одного. Порядок связи равен разности чисел электронов на связывающих и разрыхляющих орбиталях, делённой на два. В молекуле азота порядок связи равен трём:
🔥 Видео
Химия 8 класс — Ионная Связь // Химическая Связь // Подготовка к ЕГЭ по ХимииСкачать

Реакция на результаты ЕГЭ 2022 по русскому языкуСкачать

Химическая связь. Формулы Льюиса. 8 класс.Скачать

Энергетические уровни. 8 класс.Скачать

Органическая Химия — ЭТО НУЖНО ВИДЕТЬ! Гибридизация орбиталейСкачать

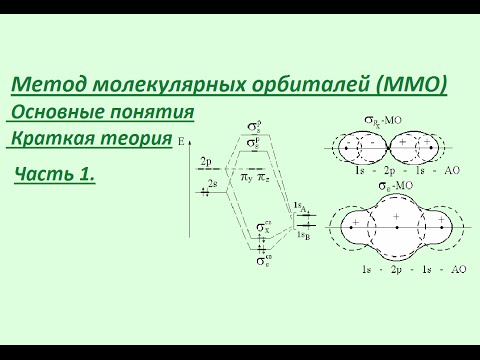
Метод молекулярных орбиталей. Часть 1. Основные понятия.Скачать
Движение электронов в атоме. 1 часть. 8 класс.Скачать

Электронные конфигурации | Химия ЕГЭ | УмскулСкачать

5. Строение вещества. Атомы и молекулы (часть 1)Скачать

Химия 11 класс (Урок№3 - Пространственное строение молекул.)Скачать

БЕЗ ЭТОГО НЕ СДАТЬ ЕГЭ по Химии — Электронная конфигурация атомаСкачать

Ерёмин В. В. - Общая химия - Строение молекул и химические связи (Лекция 3)Скачать

Химическая связь и строение молекул, С.Ю. Шавшукова, профессор кафедры ОАПХСкачать

Все задания №20 + все задачи на погрешности. Занятие 76 | ЕГЭ по физике | Makhlin SchoolСкачать

Химия | Молекулярные и ионные уравненияСкачать

Метод молекулярных орбиталей (химическая связь, часть 3)Скачать

введение в теорию МОСкачать

Составление формул органических соединений по названиюСкачать

