Решение по химии на определение рН раствора электролита
Задача 538.
Вычислить рН растворов, в которых концентрация ионов Н+ (в моль/л) равна: а) 2 . 10-7 моль/л; б) 8,1 . 10-3 моль/л; в) 2,7 . 10-10 моль/л.
Решение:
Степень кислотности или щёлочности раствора выражается отрицательным десятичным логарифмом
концентрации водородных ионов и называется водородным показателем рН:
рН = -lg[H+]
Округляя значение логарифма до 0,01, получим:
а) рН = -lg2 . 10-7 = 7 -lg2 = 7 — 0,30 = 6,70;
б) рН = -lg8,1 . 10-3 = 3 -lg8,1 = 3 — 0,90 = 2,10;
в) рН = -lg2,7 . 10-10 = 10 -lg2,7 = 10 — 0,43 = 9,57.
Ответ: а) 6,70; б) 2,09; в) 9,57.
Задача 539.
Вычислить рН растворов, в которых концентрация ионов OH— (в моль/л) равна: а) 4,6 . 10-4 моль/л; 6) 5 . 10-6 моль/л; в) 9,3 . 10-9 моль/л.
Решение:
Зная концентрацию иона OH— можно рассчитать концентрацию ионов H+ из соотношения:
K(H2O) = [H+] . [OH—] = 10-14.
Округлив значение логарифма до 0,01, получим:
Ответ: а) 10,66; б) 8,70; в) 5,97.
Задача 540.
Вычислить рН 0,01 н. раствора уксусной кислоты, в котором степень диссоциации кислоты равна 0,042.
Решение:
Из выражения [H+] = CM рассчитаем концентрацию ионов водорода:
[H+] = 0,042 . 0,01 = 4,2 . 10-4 моль/л.
Степень кислотности или щёлочности раствора выражается отрицательным десятичным логарифмом концентрации водородных ионов и называется водородным показателем рН:
рН = -lg[H+]
Видео:Примеры решения задач на водородный показатель pH растворов. 11 класс.Скачать

Округляя значение логарифма до 0,01, получим:
рН = -lg4,2 . 10-4 = 4 -lg4,2 = 4 — 0,62 = 3,38;
Ответ: 3,38.
Задача 541.
Определить рН раствора, в 1 л которого содержится 0,1 г NаОН. Диссоциацию щелочи считать полной.
Решение:
Так как едкий натр – сильный электролит, который в водных растворах диссоциирует полностью, то концентрация гидроксид-ионов равна концентрации раствора. Находим молярную концентрацию раствора:
Находим pOH раствора:
pOH = -lg[OH—] = -lg2,5 . 10-3 = 3 -lg2,5 = 3 — 0,40 = 2,60.
Так как pH + pOH = pH2O, то получим:
pH + pOH = 14; pH = 14 — pOH = 14 — 2,6 = 11,4.
Ответ: = 11,4.
🔍 Видео
Примеры решения задач на водородный показатель pH растворов. 11 класс.Скачать

Расчет рН растворов сильных и слабых кислот. Химия для поступающих.Скачать

Расчет рН растворов сильных и слабых оснований. Химия для поступающих.Скачать

Вычисление рН в растворах солейСкачать

Примеры решения задач на водородный показатель pH растворов. 11 класс.Скачать
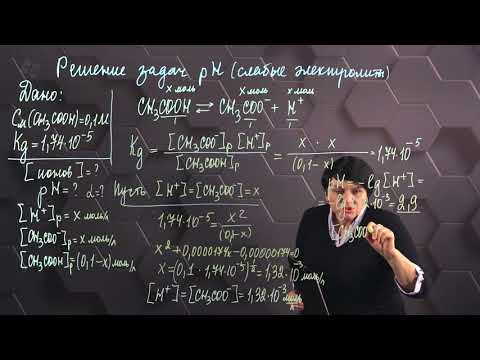
Решение задачи на pH | Химия ЦТ, ЦЭ, ЕГЭ | Решение задач по химии | Химия для школьниковСкачать

Расчёты pH буферных растворов (видео 5) | Буферные растворы | ХимияСкачать

Особые случаи pH растворов. Решение задач на рН.Скачать

Задача1Скачать

Константа кислотности (Ка) и рН для слабых кислот pH=1/2(lgKa-lg[HA])Скачать
![Константа кислотности (Ка) и рН для слабых кислот pH=1/2(lgKa-lg[HA])](https://i.ytimg.com/vi/joRCWgvvlXs/0.jpg)
Буферные растворы. Практическая часть. 11 класс.Скачать

Определение рН потенциометрическим методомСкачать

Задача на приготовление растворов методом "КРЕСТА". Включает См и массовую долю р-ров.Скачать

Способы выражения концентрации растворов. 8 класс.Скачать

pH растворов | Основные понятия | Олимпиадные задачи по химииСкачать

pH раствора солиСкачать

pH и буферные растворы | Медицинская химия | МедвузаСкачать

Лабораторный опыт №1 «Определение рН растворов кислот, щелочей» 9 классСкачать

Вывод формулы для расчета pH буферного раствораСкачать

