Энергетическая схема образования молекулярных орбиталей иона
Задача 802.
Написать в ионно-молекулярной форме уравнение реакции гидролиза Na2O2. Сохранит ли раствор Na2O2 свои белящие свойства, если его прокипятить?
Решение:
Взаимодействие пероксида натрия с водой представляет собой гидролиз соли, образованной сильным основанием (NaOH) и слабой кислотой (Н2О2) и, поэтому гидролизующейся по аниону:
Na2O2 ⇔ 2Na+ + 2O—;
Ионно-молекулярная форма процесса:
O22- + 2H2O ⇔ H2O2 + 2OH—;
Молекулярная форма процесса:
Na2O2 + 2H2O ⇔ 2H2O2 + 2NaOH.
Поскольку кислотные свойства Н2О2 выражены слабо, пероксиды, растворяясь в воде, подвергаются почти полному гидролизу. Образующийся пероксид водорода в щелочном растворе быстро разлагаются на воду и кислород. На выделении Н2О2 при этой реакции основано использование Na2O2 для отбелки различных материалов. Для этого нужно осторожно растворить пероксид натрия в холодной воде, получается раствор, содержащий гидроксид натрия и пероксид водорода, При кипячении белья в таком растворе Н2О2 разлагается на воду и кислород. Именно, в момент выделения кислорода и происходит отбеливание ткани за счёт окисления кислородом веществ, загрязняющих её, а NaOH действует как моющее средство. После кипячения раствора пероксида натрия весь пероксид водорода разлагается, и раствор, поэтому не сохраняет отбеливающие свойства.
Задача 803.
Закончить уравнения реакций:
Решение:
Задача 804.
Какие из перечисленных ионов и молекул не могут существовать: а) H22+; б) H2+; в) Н2; г) H2—; д) H22-? Потому что: 1) кратность связи равна нулю; 2) нарушается принцип Паули; 3) кратность связи меньше единицы.
Решение:
а) Энергетическая схема образования молекулярных орбиталей иона H22+ имеет вид:
При образованииH22+ из двух ионов Н+ образуется молекулярная орбиталь, на которой нет электронов, так как ионы Н+ не имеют электронов. Порядок связи данной частицы равен нулю, так как на разрыхляющией и связывающей орбиталях нет электронов. Частица не существует, так как связи нет.
б) Энергетическая схема образования молекулярных орбиталей иона H2+ имеет вид:
При образовании H2+ из атома водорода и иона водорода образуется молекулярная орбиталь на которой содержится один электрон на связывающей орбитали. Порядок связи данной частицы равен 0,5 [(1 — 0)/2 = 0,5]. Следовательно, образование будет сопровождаться выделением энергии – ион может существовать.
в) Энергетическая схема образования молекулярных орбиталей иона Н2 имеет вид:
При образовании Н2 из двух атомов водорода образуется молекулярная орбиталь на которой содержится два электрона на связывающей орбитали. Порядок связи данной частицы равен 1 [(2 — 0)/2 = 1]. Следовательно, образование Н2 будет сопровождаться выделением энергии – частица может существовать.
г) Энергетическая схема образования молекулярных орбиталей иона H2— имеет вид:
При образовании H2— из атома водорода и иона Н- образуется молекулярная орбиталь на которой содержится два электрона на связывающей орбитали и один на разрыхляющей. Порядок связи данной частицы равен 1 [(2 — 1)/2 = 0,5]. Следовательно, образование 2H- будет сопровождаться выделением энергии – частица может существовать.
д) Энергетическая схема образования молекулярных орбиталей иона H22- имеет вид:
При образовании H22- из двух ионов Н— образуется молекулярная орбиталь на которой содержится два электрона на связывающей орбитали и два на разрыхляющей. Порядок связи данной частицы равен 0 [(2 — 2)/2 = 0]. Следовательно, образование не будет сопровождаться выделением энергии – частица не может существовать.
Таким образом, ионы H22+ и H22- не могут существовать, потому что кратность связи равна нулю, значит, образование молекулярных орбиталей не будет сопровождаться выделением энергии.
Ответ: а1; д1.
📺 Видео
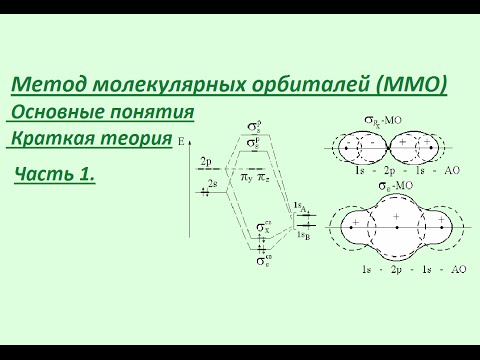
Метод молекулярных орбиталей. Часть 1. Основные понятия.Скачать
введение в теорию МОСкачать

Гибридизация атомных орбиталей и геометрия молекул. 10 класс.Скачать

Химия 8 класс (Урок№4 - Атомы, молекулы и ионы. Простые и сложные вещества.Химические элементы.)Скачать

Движение электронов в атоме. 1 часть. 8 класс.Скачать

Урок 61. Первое знакомство с методом молекулярных орбиталей.Скачать

Метод молекулярных орбиталей (химическая связь, часть 3)Скачать

Леменовский Д. А. - Неорганическая химия I - Метод молекулярных орбиталейСкачать

Атомы и молекулы. Простые и сложные вещества. 7 класс.Скачать

Молекулярные орбиталиСкачать
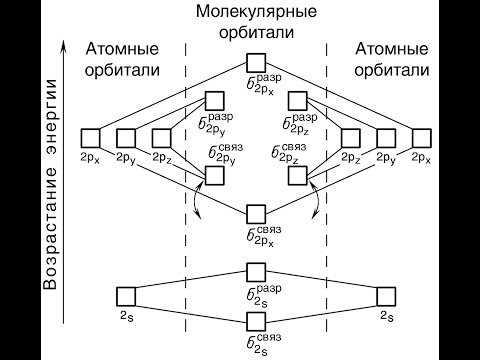
Спектр излучения водорода (видео 12) | Квантовая физика | ФизикаСкачать
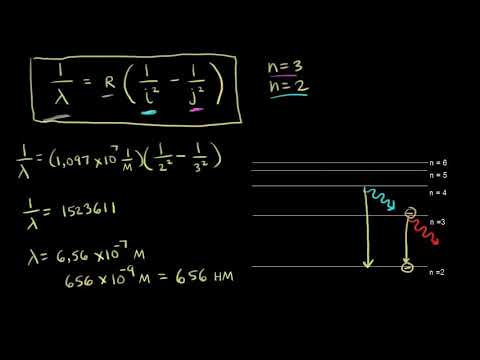
Строение молекул ч. 3 Молекулярные орбитали и computational chemistryСкачать

Неорганическая химия: ТМО и ТВС(Теория молекулярных орбиталей и Теория валентных связей)|КДО КНИТУСкачать

Урок 141. Количество вещества. Молярная масса. Оценка размеров молекулСкачать

Что такое орбитальСкачать

Нуклиды. Изотопы. Массовое число атома. Урок 17. Химия 8 классСкачать

Кислотно-основное равновесие. Буферные растворы. pH растворов.Скачать

Атомно-молекулярное учение. Видеоурок 6. Химия 8 классСкачать

Квантовые числа и атомные орбитали. 10 класс.Скачать

5. Строение вещества. Атомы и молекулы (часть 1)Скачать

