Составление электронных формул элементов исходя из положения их в таблице Д.И. Менделеева
Электронные структуры атомов марганца и брома
Задача 4
Исходя из электронных структур атомов марганца и брома, их места в периодической системе, объясните сходство и различие их химических свойств.
Решение:
Марганец — 25 –й элемент таблицы Менделеева. Электронная формула марганца имеет вид:
1s2 2s2 2p6 3s2 3p6 4s2 3d5
Валентные электроны находятся на 4s и 3d подуровнях. На валентных орбиталях атома марганца находится 7электронов.
Бром – 35 элемент периодической таблицы Электронная формула брома имеет вид:
1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p5
Валентные электроны находятся на 4s и 4р подуровнях. На валентных орбиталях атома находится 7 электронов.
Таким образом, марганец и бром не являются электронными аналогами и не должны размещаться в одной и той же подгруппе. Но на валентных орбиталях атомов этих элементов находится одинаковое число электронов – 7. Поэтому оба элемента помещают в одну и ту же группу периодической системы Д.И.Менделеева. Марганец – d-элемент VIIB-группы, а бром – p-элемент VIIA-группы.
На внешнем энергетическом уровне у атома марганца два электрона, а у брома – семь. Атомы типичных металлов характеризуются наличием небольшого числа электронов на внешнем энергетическом уровне, а следовательно, тенденцией терять эти электроны. Они обладают только восстановительными свойствами и не образуют элементарных отрицательных ионов. Элементы, атомы которых на внешнем уровне содержат более трех электронов, обладают определенным сродством к электрону, а следовательно, приобретают отрицательную степень окисления и даже образуют элементарные отрицательные ионы. Таким образом, марганец, как и все металлы, обладает только восстановительными свойствами, тогда как для брома, проявляющего слабые восстановительные свойства, более свойственны окислительные функции. Общей закономерностью для всех групп, содержащих p- и d-элементы, является преобладание металлических свойств у d-элементов. Следовательно, металлические свойства у марганца сильнее выражены, чем у брома.
Электронная формула ванадия
Задача 5.
Напишите электронно-графическую формулу для 23 элемента, определите его валентные электроны и охарактеризуйте их с помощью квантовых чисел.
Решение:
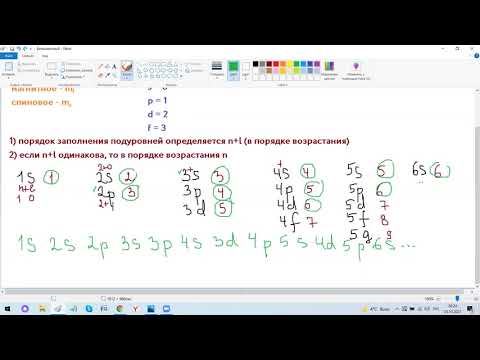
Электронные формулы отображают распределение электронов в атоме по энергетическим уровням, подуровням (атомным орбиталям). Электронная конфигурация обозначается группами символов nlx, где n – главное квантовое число, l – орбитальное квантовое число (вместо него указывают соответствующее буквенное обозначение – s, p, d, f), x – число электронов в данном подуровне (орбитали). При этом следует учитывать, что электрон занимает тот энергетический подуровень, на котором он обладает наименьшей энергией – меньшая сумма n+1 (правило Клечковского). Последовательность заполнения энергетических уровней и подуровней следующая:
1s>2s>2р>3s>3р>4s>3d>4р>5s>4d>5р>6s>(5d1) >4f>5d>6р>7s>(6d1-2)>5f>6d>7р
Так как число электронов в атоме того или иного элемента равно его порядковому номеру в таблице Д.И. Менделеева, то для 23 элемента — ванадия( V –порядковый № 23) электронная формула имеют вид:
V23 1s22s22р63s23р64s23d3
Валентные электроны ванадия — 4s23d3 — находятся на 4s и 3d подуровнях На валентных орбиталях атома ванадия находится 5 электронов. Поэтому элемент помещают в пятую группу периодической системы Д.И.Менделеева.
💡 Видео
11 класс.Элементы 4 периода.Электронные формулы.Скачать

8 класс. Распределение электронов в атоме. Электронные формулы.Скачать

Электронные формулы d-элементов. Явление проскока электрона.Скачать

Как быстро составить электронную конфигурацию атома? [Лайфхак] Урок 5Скачать
![Как быстро составить электронную конфигурацию атома? [Лайфхак] Урок 5](https://i.ytimg.com/vi/_t7st9JNAGA/0.jpg)
Строение атома. Как составить электронную и электронно-графическую формулы?Скачать

ХИМИЯ ПРОСТО — Электронная конфигурация атомаСкачать

БЕЗ ЭТОГО НЕ СДАТЬ ЕГЭ по Химии — Электронная конфигурация атомаСкачать

Возбужденное состояние атома | Химия ЕГЭ | УмскулСкачать

Электронная конфигурация атома "Проскок электрона"Скачать

Электронные конфигурации | Химия ЕГЭ | УмскулСкачать

Электронные формулы атомов (практика). Учимся составлять электронные формулы атомов.Скачать

Электронная формула. Ряд КлечковскогоСкачать
Электронные конфигурации атомов. Химия – простоСкачать

Валентность. Учимся определять валентность элементов по формуламСкачать

Подсчет валентных электронов (видео 3) | Периодическая таблица| ХимияСкачать

Энергетические уровни. 8 класс.Скачать

ПЕРИОДИЧЕСКАЯ СИСТЕМА И СТРОЕНИЕ АТОМАСкачать

Как решать 1 задание из ЕГЭ по химии "Электронная конфигурация атома"Скачать

СОЕДИНЕНИЯ МАРГАНЦА IV и VII | Таисия Фламель | ВебиумСкачать

Электронные конфигурации первых 36 элементов для задания 1 | Химия ЕГЭ УМСКУЛ Богдан ЧагинСкачать

