Задача 119.
Навеску извести массой 0,7500 г обработали 100 см3 0,1 М раствора HCl; избыток кислоты оттитровали 20,00 см3 раствора NaOH с титром 0,004216 г/см3. Вычислите содержание СаО в извести (w, %).
Решение:
a(СаО) = 0,7500 г;
V(HCl) = 100 см3;
CM(HCl) = 0,1 М;
V(NaOH) = 20,00 см3;
Э(NaOH) = 40 г/моль;
Э(СаО) = 28 г/моль;
T(NaOH) = 0,004216 г/см3;
w%(CaO) = ?
Уравнение реакции имеет вид:
CaO + 2HCl = СаCl2 + Н2О;
NaOH + HCl = NaCl + H2O
Определяемое вещество (А) – CaO; М = 56 г/моль; Титранты: HCl (B1) и NaOH (В2), их молярные концентрации равны нормальным.
- 1. Расчет нормальности раствора второго титранта
- 2. Расчет массы определяемого вещества в навеске образца
- 3. Расчет массовой доли определяемого вещества в навеске пробы
- Вычисление массы азотной кислоты
- 1. Расчет нормальности раствора титрана
- 2. Расчет нормальности раствора определяемого вещества
- 3. Расчет массы кислоты в 250 см3 ее раствора
- Анализ буры методом титрования
- 1. Рассчитаем массу буры, содержащейся в навеске образца
- 💡 Видео
1. Расчет нормальности раствора второго титранта
Нормальность раствора NaOH рассчитаем по формуле:
СН(В) = [Т(В) · 1000]/Э(B), где
Видео:Полный гайд по титрованию с Игнатом Тарабриным | AllesСкачать

Т(В) — титр раствора титранта; Э(B) — эквивалентная масса титранта.
Тогда
СН(NaOH) = [Т(NaOH) · 1000]/Э(NaOH) = (0,004216 · 1000)/40 = 0,1054 моль.
2. Расчет массы определяемого вещества в навеске образца
Массу (m) CaO определяем по формуле:
m(A) = [CH(B1)V(B1) — CH(B2)V(B2)]Э(А)/1000,
CH(B1) — нормальность раствора первого титранта; CH(B2) — нормальность раствора второго титранта; V(B1) — объем раствора первого титранта; V(B2) — объем раствора второго титранта; Э(А) — эквивалентная масса определяемого вещества.
Тогда
m(СаО) = [CH(HCl)V(HCl) — CH(NaOH)V(NaOH)]Э(А)/1000 = (0,1 · 100) — [(0,1054 · 20,00)]28/1000 = 0,2210 г.
3. Расчет массовой доли определяемого вещества в навеске пробы
Массовую долю СаО в навеске извести, рассчитаем по формуле:
Видео:Введение в титрование (видео 1)| Титриметрический анализ | ХимияСкачать

w% = (m · 100%)/a, где
а — навеска вещества; m — масса определяемого вещества.
Тогда
w% (СаО) = (0,2210 · 100%)/0,7500 = 29,47%.
Ответ:w% (СаО) = 29,47%.
Вычисление массы азотной кислоты
Задача 120.
Азотную кислоту неизвестной концентрации разбавили в мерной колбе вместимостью 250 см3. На титрование 25,00 см3 полученного раствора израсходовано 32,00 см3 раствора NaOH с T(NaOH/HNO3) равным 0,063000 г/см3. Вычислите массу HNO3.
Решение:
V(к) = 250 см3;
V(HNO3) = 25,00 см3;
V(NaOH) = 32,00 см3;
T(NaOH/HNO3) = 0,063000 г/см3;
Э(NaOH) = 40 г/моль;
Э(HNO3) = 63 г/моль;
m(HNO3) = ?
Уравнение реакции имеет вид:
HNO3 + NaOH = NaNO3 + H2O
HNO3 – определяемое вещество (А); NaOH – титрант (В).
1. Расчет нормальности раствора титрана
Видео:Определение концентрации вещества в растворе методом титриметрииСкачать

Нормальность раствора NaOH рассчитаем по формуле:
СН(В) = [T(B/A) · 1000]/Э(A), где
СН(В) — нормальность раствора титранта; T(B/A) — титр раствора по определяемому веществу; Э(A) — эквивалентная масса титранта.
Тогда
СН(NaOH) = [T(NaOH/HNO3) · 1000]/Э(HNO3) = (0,063000 · 1000/63 = 1 Н.
2. Расчет нормальности раствора определяемого вещества
Нормальность раствора HNO3 рассчитаем по формуле:
СН(А) = [СН(В) · V(В)]/V(А), где
СН(А) — нормальность раствора определяемого вещества; V(В) — объем раствора титранта; V(A) — объем раствора определяемого вещества.
Тогда
Видео:Определение рН потенциометрическим методомСкачать

СН(HNO3) = [СН(NaOH) · V(NaOH)]/V(HNO3) = (1 · 32)/25 1,28 Н.
3. Расчет массы кислоты в 250 см3 ее раствора
Массу HNO3 находим по формуле:
m = [V(к) · СН(А) · Э(A)]/1000, где
V(к) — объем анализируемого раствора; СН(А) — нормальность раствора определяемого вещества; Э(A) — эквивалентная масса определяемого вещества.
Тогда
m(HNO3) = [V(к) · СН(HNO3) · Э(HNO3)]/1000 = (250 · 1,28 · 63)/1000 = 20,16 г.
Ответ: m(HNO3) = 20,16 г.
Анализ буры методом титрования
Задача 121.
На титрование образца технической буры массой 0,2298 г израсходовано 10,60 см3 0,106 М раствора HCl. Определите содержание Na2B4O7 · 10H2O в образце (w, %).
Решение:
а(Na2B4O7 · 10H2O) = 0,2298 г;
V(HCl) = 10,60 см3;
CM(HCl) = 0,106 М;
w%(Na2B4O7 · 10H2O) = ?
Определяемое вещество (А) – Na2B4O7 · 10H2O; М = 381,37 г/моль; Э = 190,685 г/моль. Титрант: HCl
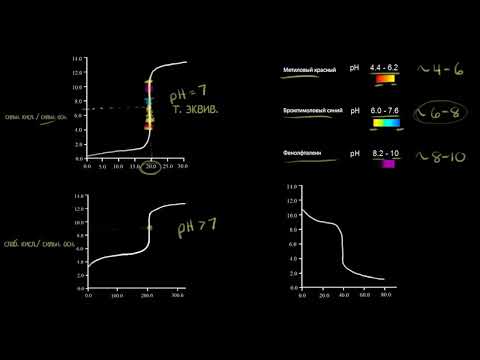
Видео:Кривые титрования и кислотно-основные индикаторы (видео 14) | Титриметрический анализ | ХимияСкачать
Уравнение реакции:
Na2B4O7 · 10H2O + 2HCl → 2NaCl + 4H3BO3 + 5H2O.
1. Рассчитаем массу буры, содержащейся в навеске образца
Массу Na2B4O7 · 10H2O рассчитаем по формуле:
m = [СН(B) · V(B) · Э(А)]/1000, где
CH(B) — нормальность раствора титранта; V(B) — объем раствора титранта, см3; Э(A) — эквивалентная масса определяемого вещества.
Тогда
m(Na2B4O7 · 10H2O) = [CH(HCl) · V(HCl) · Э(Na2B4O7 · 10H2O)]/1000 =
= (0,106 · 10,60 · 190,685)/1000 = 0,21425 г.
Искомую величину w, %, находим по формуле:
w% = (m · 100%)/a, где
Видео:Кислотно-основное титрование. 11 класс.Скачать

m — масса определяемого вещества А, г; a — навеска вещества, г
Тогда
w%(Na2B4O7 · 10H2O) = [m(Na2B4O7 · 10H2O) · 100%]/a =
= (0,21425 · 100%]/0,2298 = 93,24 %.
Ответ: w%(Na2B4O7 · 10H2O) = 93,24 %.
💡 Видео
Задача на кислотно-основное титрование (видео 16) | Титриметрический анализ | ХимияСкачать

Окислительно-восстановительное титрование (видео 17) | Титриметрический анализ | ХимияСкачать
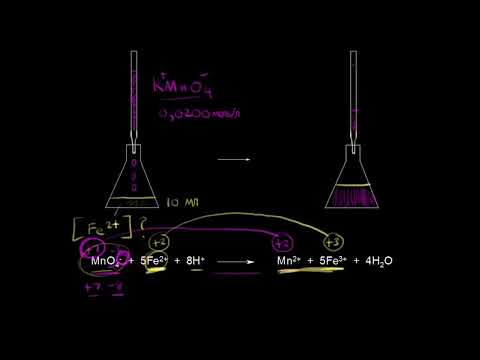
Окислительно-восстановительное титрование: перманганатометрия.Скачать

Кислотно основное титрованиеСкачать

Кислотно-основное титрование многоосновных кислот и их солей. Часть 1.Скачать

Потенциометрическое титрованиеСкачать

КОТ. Техника работы с мерной посудой. Основы титриметрического анализа.Скачать

Титрование слабого основание сильной кислотой. Часть 1 (видео 7) | Титриметрический анализ | ХимияСкачать
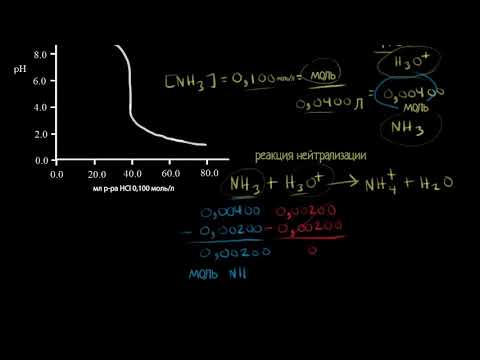
Как правильно титровать? Найдите типичные ошибкиСкачать

Лекция 3. Кислотно-основное титрование.Скачать

Кислотно-щелочное титрованиеСкачать

Титрование слабой кислоты сильным основанием. Часть 1 (видео 5)| Титриметрический анализ | ХимияСкачать

Осадительное титрование.Скачать

Титр раствора (Т). Решение задач. Часть 1.Скачать

